Ранее: Энтропия пекарских дрожжей
В предыдущей заметке была рассмотрена термодинамика реакции метаболизма при росте пекарских дрожжей, при этом особое внимание было уделено энтропии сухой биомассы дрожжей. В этой заметке рассматривается производство энтропии и диссипация энергии Гиббса в реакциях метаболизма на основе работ Урса фон Стокара. Предложенная им концептуальная модель проточного реактора идеального смешения, с одной стороны, является достаточно простой, а с другой, она включает в себя все основные компоненты неравновесной термодинамики, необходимые для понимания энергетики метаболизма при росте микроорганизмов.
Рассмотрение проведено на качественном уровне при использовании минимального количества уравнений без вывода. Основное внимание уделено концептуальным вопросам. Разнообразие метаболизмов в разных группах микроорганизмов позволяет провести обсуждение связи производства энтропии и диссипации энергии Гиббса при росте микроорганизмов с двумя факторами: теплотой, выделяющейся в ходе метаболизма, и изменением энтропии в реакции метаболизма.
- Закрытая система при постоянных температуре и давлении
- Живая клетка как проточный реактор идеального смешения
- Микробы и отрицательная энтропия Шрёдингера
- Физический смысл производства энтропии
Закрытая система при постоянных температуре и давлении
Вначале кратко рассмотрим простой пример из раздела ‘Расчет равновесного состава при заданных температуре и давлении‘ главы ‘Адиабатическая температура пламени‘. Рассматриваемая реакция далека от метаболизма, но этот пример позволяет вспомнить базовые концепции химической термодинамики, необходимые для следующих разделах: энергия Гиббса системы, химическая переменная, энергия Гиббса химической реакции, максимальная полезная работа и производство энтропии.
Рассмотрим закрытую систему, в которой протекает одна реакция при заданных внешних температуре и давлении:
| CO2 | = | СO | + | 0.5O2 |
| 1 − ξ | ξ | 0.5ξ |
Предполагается, что в начальном состоянии системы находился один моль CO2. Протекание реакции характеризуется химической переменной ξ, которая показывает число молей распавшегося CO2 и одновременно число молей появившихся продуктов диссоциации. При заданных условиях энергия Гиббса системы является критерием самопроизвольного процесса: энергия Гиббса системы стремится к минимуму. Для наглядности ниже приведен рисунок, показывающий изменение энергии Гиббса системы как функции химической переменной при 2518 К и 1 атм:
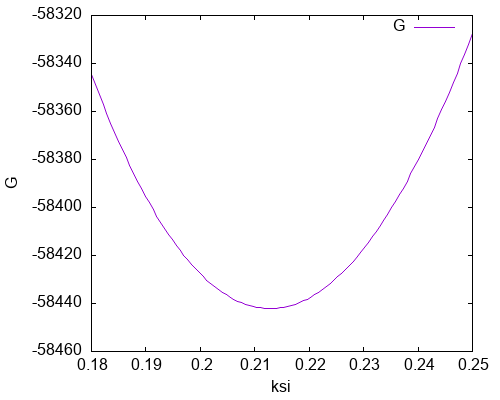
На рисунке приведен диапазон значений химической переменной, близкий к минимальному значению (ξ = 0.213), при котором достигается равновесное состояние. Рассмотрим производную энергии Гиббса системы по химической переменной. Можно доказать, что она равна энергии Гиббса реакции при данных температуре, давлении и концентрации веществ:
(∂G/∂ξ) = ΔrG = Gm(CO) + 0.5Gm(O2) ‐ Gm(CO2)
Энергия Гиббса реакции является разностью парциальных энергий Гиббса продуктов и реагентов, взятых с необходимыми стехиометрическими коэффициентами. При изменении химической переменной концентрации меняются и тем самым энергия Гиббса реакции также меняется.
На графике энергия Гиббса реакции является касательной к приведенной кривой энергии Гиббса системы (свойство производной). На левой части кривой от состояния равновесия энергии Гиббса реакция отрицательна, и реакция протекает слева направо. На правой части кривой энергия Гиббса реакции становится положительной, и реакция протекает справа налево. Таким образом любое начальное состояние системы заканчивается состоянием равновесия, в котором энергия Гиббса реакции равна нулю.
При переходе из одного состояния в другое изменение энергии Гиббса всей системы при постоянных внешних температуре и давлении связана с максимальной полезной работой, которая достигается при использовании обратимых процессов:
‐ΔG = ‐(G2 ‐ G1) = Wmax
Обратимые термодинамические процессы являются идеализацией и недостижимы на практике; поэтому реальная работа (W) всегда меньше максимальной. В технической термодинамике для сохранения равенства вводится понятие потерянной работы (Wmax = W + Wloss). При этом, согласно теореме Гуи-Стодола, в ходе такого изменения потерянная работа связана с производством энтропии:
‐ΔG = W + Wloss = W + TSgen
Введение производства энтропии дает количественную связь между энтропией и диссипацией энергии в реальных необратимых процессах. Это позволяет использовать производство энтропии для оптимизации энергетических процессов. Перед инженерами ставится задача по возможности уменьшить диссипацию энергии, что соответствует минимизации производства энтропии.
Производство энтропии, как и работа, не является функцией состояния, поэтому в уравнении выше перед работой и производством энтропии нельзя поставить символ Δ. Работа и производство энтропии являются функцией процесса; например, в обратимом процессе производство энтропии равно нулю.
Живая клетка как проточный реактор идеального смешения
Живая клетка является открытой системой, но в хорошем приближении клетка находится при постоянных температуре и давлении. Ниже приведен рисунок из статьи фон Стокара, который показывает, что в клетку поступают вещества, из клетки выходят продукты реакции, а также происходит теплообмен с окружающей средой.

В статье фон Стокара предлагается упростить рассмотрение происходящих химических превращений путем игнорирования внутренней структуры клетки. При рассмотрении термодинамики реакции такое допущение вполне допустимо, поскольку изменение термодинамических свойств не зависит от механизмов протекающих реакций. Можно провести аналогию с изучением эффективности использования топлива в двигателе внутреннего сгорания. Термодинамика позволяют оценить эту эффективность без знания механизмов горения топлива и в этом заключается преимущество термодинамического анализа.
В статье фон Стокара приведены выкладки, которые исходя из рисунка выше переходят к рассмотрению проточного реактора идеального смешения, используемого для роста микроорганизмов. Рассмотрим схему из Википедии (Continuous stirred-tank reactor):
Приведу реакцию метаболизма роста дрожжей на глюкозе из предыдущей заметки:
C6H12O6(aq) + 0.302NH3(aq) + 4.050O2(aq) + 0.023H3PO4(aq) + 0.006H2SO4(aq) = 1.914CH1.613O0.557N0.158P0.012S0.003(biomass) + 4.086CO2(aq) + 4.950H2O(l)
В реакторе идеального смешения предполагается, что концентрация любого вещества в данный момент времени одинакова в любой точке реактора. Реагенты постоянно подаются в реактор, а продукты реакции выводятся из реактора. Таким образом происходит безостановочное производство биомассы. Вся система остается при постоянных температуре и давлении, поскольку теплота реакции также отводится из реактора в окружение.
В стационарном состоянии существенно упрощаются уравнения, описываемые работу реактора. Стационарность состояния означает, что приток и отток веществ полностью соответствует изменению химической переменной в протекающей реакции. В результате реакция проходит, а концентрации веществ в реакторе не меняются во времени. В этом случае изменение энергии Гиббса такой системы совпадает с изменением энергии Гиббса протекающей реакции.
Выкладки фон Стокара приводят к связи между производством энтропии и энергией Гиббса реакции. Перед этим напомню, что метаболизм объединяет две реакции. Реакция распада субстрата (катаболизм) протекает самопроизвольно, а реакция роста биомассы (анаболизм) энергетически невыгодна. Таким образом, часть энергии Гиббса реакции катаболизма используется для роста биомассы. В этом смысле «полезная химическая работа» уже включена в реакцию метаболизма. Выражение «полезная химическая работа» приведено в кавычках, поскольку оно использовано по аналогии с полезной работой в инженерной термодинамике, но формально не является работой.
В то же время в ходе роста биомассы не производится полезная работа в смысле инженерной термодинамики и поэтому потерянная работа формально равна максимальной полезной работе. Таким образом, в конечном уравнении, которое напоминает уравнение из предыдущего раздела, остается только производство энтропии:
‐ΔrG = TSgen
Это уравнение можно записать через производные по времени: слева производная по времени от химической переменной, справа производная по времени от производства энтропии. Однако для последующего обсуждения удобнее рассмотреть разницу между двумя состояниями реактора при изменении химической переменной на один моль. Это соответствует одному пробегу реакции и тогда энергия Гиббса реакции равна производству энтропии в таком изменении с обратным знаком.
Минимальное производство энтропии соответствует состоянию равновесию (ΔrG = 0), но в этом случае реакция не идет. В реальных процессах диссипация энергии неизбежна и в данном случае энергии Гиббса реакции является мерой диссипации энергии. Напомню, что отрицательная энергия Гиббса означает только возможность протекания реакции, а реальное протекание реакции зависит от кинетики процесса. Нельзя забывать, что протекающие процессы в живой клетке крайне сложны и что реальная скорость определяется этими процессами.
Микробы и отрицательная энтропия Шрёдингера
Эрвин Шрёдингер ввел в обиход выражение ‘Организм питается отрицательной энтропией‘ и среди биологов были и идут долгие споры о значении сказанного Шрёдингером. Название статьи фон Стокара ‘Всегда ли микроорганизмы питаются отрицательной энтропией?‘ отражает это обстоятельство. В статье выбрана одна из интерпретаций слов Шрёдингера, связанная с энтропией реакции метаболизма. Предполагается, что тайный смысл утверждения Шрёдингера связан с увеличением энтропии в ходе реакции метаболизма. Другими словами, питание отрицательной энтропией считается эквивалентным положительной энтропии реакции метаболизма.
Энергия Гиббса реакции связана с энтальпией и энтропией реакции:
‐TSgen = ΔrG = ΔrH ‐ T ΔrS
Если поделить обе части уравнения на температуру, то получится связь производства энтропии с энтальпией и энтропией реакции. Это показывает, что существуют два разных фактора, которые определяют производство энтропии при протекании химической реакции. Это теплота протекающей реакции (энтальпийный фактор) и энтропия реакции (энтропийный фактор). В статье фон Стокара обсуждается непосредственно диссипация энергии Гиббса, то есть, рассматривается уравнение выше без перехода к производству энтропии.
Энергия Гиббса самопроизвольной химической реакции должна быть отрицательной (производство энтропии всегда положительно), но при этом возможны разные соотношения между энтальпийным и энтропийным факторами. Существуют самые разные микроорганизмы и были найдены четыре группы реакций метаболизма роста микроорганизмов, показанные на рисунке ниже:

Слева показана энергия Гиббса реакции, значение которой для наглядности нормировано на одинаковое значение для всех четырёх рассмотренных случаях. Для понимания графика следует обратить внимание, что энергия Гиббса отрицательна — столбик расположен ниже нуля. Таким образом вклады в энергию Гиббса также должны быть отрицательными. Для экзотермических реакций с выделением теплоты в окружающую среду энтальпия реакции отрицательна и ΔrH непосредственно входит в отрицательную энергию Гиббса. Энтропия реакции входит в энергию Гиббса с отрицательным знаком и поэтому положительная энтропия реакции соответствует правильному вкладу в отрицательную энергию Гиббса реакции.
Справа находятся две колонки, в которых диссипация энергии Гиббса определяется преимущественно энтальпией реакции. Во втором столбике справа (Aerobic respiration — аэробное дыхание) в том числе находится метаболизм роста дрожжей на глюкозе в присутствии кислорода. В этом случае энтальпия реакции является основной составляющей энергии Гиббса, а энтропия реакции играет незначительную роль.
Первый столбик справа связан с ростом микроорганизмов в присутствии углекислого газа и водорода, в ходе которого получается метан [Methanogenesis on (CO2+H2) — метаногенез на основе (CO2+H2)]. Энтропия такой реакции метаболизма отрицательна: энтропия продуктов меньше, чем энтропия реагентов, что противоречит идее Шрёдингера. В этом случае энтальпия реакции перевешивает неправильный энтропийный вклад.
Два столбика слева ближе к интерпретации Шрёдингера, поскольку энтропия реакции играет существенно большую роль. Во второй столбик слева (Fermentation — ферментация) входит в том числе метаболизм в ходе брожения под действием дрожжей, то есть, рост дрожжей на глюкозе в отсутствии кислорода. В этом случае энтропийный вклад в энергию Гиббса (или в производство энтропии) значительно превышает энтальпийный вклад.
Столбик рядом (Methanogenesis on acetate — метаногенез на основе ацетата) соответствует эндотермической реакции метаболизма. Рост микроорганизмов в этом случае требует притока теплоты из окружения. В этом столбике энтропийный вклад компенсирует неправильный энтальпийный вклад.
Рисунок выше показывает, что даже в такой интерпретации загадочных слов Шрёдингера приходится сказать, что Шрёдингер полностью проигнорировал энтальпийный вклад в производство энтропии. Это в свою очередь дает еще один повод не принимать рассмотрение Шрёдингера всерьез.
Физический смысл производства энтропии
В свое время Больцман выдвинул идею о важности энтропии в биологии:
‘Поэтому всеобщая борьба за существование живых существ не является борьбой за составные элементы … или за энергию … Но это — борьба за энтропию, которую можно использовать при переходе энергии с горячего солнца к холодной земле.’
Шрёдингер, по всей видимости, в своем рассмотрении отталкивался от этих слов Больцмана:
‘Так, живой организм непрерывно повышает свою энтропию – или, можно сказать, производит положительную энтропию, – тем самым стремясь к опасному состоянию максимальной энтропии, то есть смерти. Чтобы держаться подальше от этого состояния – то есть жить, – организму необходимо постоянно черпать из окружающей среды отрицательную энтропию.’
Это привело к распространению «мистических» взглядов на энтропию, когда энтропии и производству энтропии приписывается решающая роль в жизни организма.
Полезно с этой точки зрения вернуться к теореме Гуи-Стодола. Развитие термодинамики связано с рассмотрением идеального теплового двигателя на основе обратимых термодинамических процессов, когда достигается максимальный коэффициент полезного действия (к.п.д.). Правда, обратимые процессы являются идеализацией и при прохождении реальных процессов к.п.д. двигателя всегда меньше идеального значения.
В этом смысле потерянная работа характеризует упущенные возможности при прохождении реальных процессов по сравнению с идеализированными обратимыми процессами. Таким образом, производство энтропии точно также является характеристикой упущенных возможностей. Другими словами, физический смысл производства энтропии заключается в сравнении реального и идеализированного.
Введение потерянной работы является полезным шагом при инженерных разработках, поскольку это вводит показатель, необходимый для оптимизации промышленных устройств. В неравновесной термодинамике появляются выражения для производства энтропии для ряда процессов и таким образом теорема Гуи-Стодола позволяет использовать эти выражения при оптимизации производства.
Рассмотрим построение неравновесной термодинамики. Производство энтропии выводится из уравнения баланса энтропии, которое добавляется к существующим уравнениям переноса и кинетическим уравнениям без их изменения. Это означает, что производство энтропии в неравновесной термодинамике не влияет на прохождение процессов. Можно решить все исходные уравнения без использования баланса по энтропии, при этом все характеристики процессов останутся без изменения. Баланс по энтропии полезен для сравнения реальных процессов с идеализированным, но это сравнение никак не влияет на протекание реальных процессов самих по себе.
Таким образом, уравнение баланса энтропии полезно для решения определенных задач, но нельзя воспринимать производство энтропии в качестве причины происходящего. Реальные процессы связаны с протеканием элементарных химических реакций, диффузии, теплообмена и т. д. Каждый из этих процессов приводит к диссипации энергии. Это означает, что можно вообразить идеализированный процесс без диссипации энергии, а далее количественно оценить диссипацию энергии посредством использования уравнения баланса энтропии. Тем не менее, оценка диссипации энергии не влияет на уравнения, определяющие протекание реальных процессов.
Энтропия системы меняется вследствие теплообмена, но нельзя сказать, что теплообмен происходит вследствие необходимости отвода энтропии. Точно также энтропия системы меняется вследствие притока веществ, протекания химической реакции, и отвода продуктов реакции. Но нельзя сказать, что происходящие химические процессы и массообмен вызываются необходимостью производства и отвода энтропии.
В этом смысле нельзя сказать, что смерть организма наступает из-за переизбытка энтропии. Смерть наступает из-за перегрева или переохлаждения организма, из-за недостатка питательных веществ, прекращения доступа кислорода или внутренних нарушений в организме, которые мешают протеканию необходимых процессов, и т. д.
Рассмотрение энтропии и производства энтропии принадлежит термодинамическому анализу протекающих процессов, который позволяет оценить эффективность использования энергии, и тем самым дает возможность сравнения эффективности. Вполне можно говорить о производстве энтропии внутри организма и отводе энтропии, как это было сделано при рассмотрении роста микроорганизмов в предыдущем разделе. Однако не следует из этого делать вывод о «мистической» связи производства энтропии с функционированием организма.
Информация
U. von Stockar, J-S. Liu. Does microbial life always feed on negative entropy? Thermodynamic analysis of microbial growth. Biochimica et Biophysica Acta (BBA)-Bioenergetics 1412, no. 3 (1999): 191-211.
Статья в открытом доступе на ScienceDirect. Два рисунка из статьи использованы для некоммерческих целей в рамках лицензии Elsevier.
Более подробное изложение этих идей:
Biothermodynamics. The role of thermodynamics in Biochemical Engineering, 2013. Urs von Stockar, chapter 16, Live cells as open non-equilibrium systems; chapter 19, Biothermodynamics of live cells.
Вывод теоремы Гуи-Стодола:
A. Bejan, Advanced Engineering Thermodynamics, 2016.
Критика отрицательной энтропии Шрёдингера (цитаты Больцмана и Шрёдингера взяты из этой статьи):
Е. Б. Рудный, Эрвин Шрёдингер и отрицательная энтропия, 2025, PREPRINTS.RU, doi.org:10.24108/preprints-3113815
